A RDC 44, traz em sua ementa original que a mesma dispõe sobre as Boas Práticas Farmacêuticas para o controle sanitário do funcionamento, da dispensação e da comercialização de produtos e da prestação de serviços farmacêuticos em farmácias e drogarias e dá outras providências. Sua publicação deu-se no ano de 2009, e seu principal objetivo é promover o uso racional de medicamentos, resgatar o direito do cidadão à informação e reduzir a automedicação e o uso abusivo de medicamentos, entre outros.
Depois de 11 anos esta norma está sendo revisada, e para compreendermos melhor o momento em que esta resolução se encontra, vale ressaltar algumas etapas, especialmente a Consulta Pública (CP): um mecanismo de participação social que submete minutas de atos normativos ao recebimento de contribuições e sugestões do público amplo, por um período determinado, podendo até ser solicitada prorrogação de prazo. As contribuições são realizadas de forma eletrônica, por meio do FormSUS disponibilizado no site da Anvisa.
As manifestações são recebidas como subsídios e informações da sociedade para a consolidação da norma, sem caráter decisório. O texto final é submetido à decisão da Diretoria Colegiada (Dicol) da Autarquia.
Vale ressaltar que o processo de revisão da RDC 44/2009 foi realizado com base em ferramentas da Análise de Impacto Regulatório (AIR), empregadas pela Agência desde 2018. Em 2019 a Autarquia promoveu, junto à às Vigilâncias Sanitárias (Visas) estaduais e municipais uma consulta dirigida, com o objetivo de levantar dados sobre a prestação de serviços de assistência à saúde em farmácias do País.
Para coletar informações precisas sobre o tema e, com isso, aprimorar a regulação voltada para este segmento, a Anvisa disponibilizou um formulário eletrônico a ser preenchido pelos profissionais das vigilâncias sanitárias que realizam a inspeção nas farmácias, na parte de serviços de saúde para o estudo.
Após a análise dos dados, constatou-se a ampliação das atividades previstas na RDC 44/2009, como a realização de curativos, serviços de estética (tratados em resoluções específicas do CFF), nebulização e a realização de testes do tipo Point-of-Care (POCT), além dos destinados à glicemia.
De acordo com a Anvisa, também em 2019, a Agência realizou uma Consulta Dirigida Internacional para conhecer o panorama dos serviços de saúde oferecidos nas farmácias de diferentes países. O questionário utilizado como instrumento de consulta foi encaminhado às autoridades de saúde de 15 países. Desses, oito responderam ao contato e seis à pesquisa (Austrália, Canadá, Chile, Coreia do Sul, Japão e Portugal). Em comparação aos regulamentos e orientações de outros países, a RDC 44/2009 é mais restritiva e detalhada sobre aspectos da atividade farmacêutica. O escopo das atividades de serviços de saúde e a realização de testes point-of-care em farmácias brasileiras, quando comparados à prática de assistência nas farmácias dos outros países, se apresentaram desatualizados.
Agora, com a CP 911/2020, estamos tratando de uma norma alteradora, que tem como fim:
- Reprodução integral em um só texto, quando se tratar de alteração considerável, revogando-se o texto anterior;
- Revogação parcial de artigos, parágrafos, incisos, alíneas ou itens; ou
- Substituição, supressão ou acréscimo de dispositivo.
A alteração de uma norma exige a elaboração de uma nova normativa, seguindo o fluxo normal de regulamentação. Portanto, a RDC 44/2009, em sua grande parte, trata do fluxo do medicamento, não sendo necessária ainda neste momento a revisão geral da norma, segundo informações da própria Anvisa por meio de um Webinar realizado no dia 22 de setembro de 2020. Entretanto, naturalmente ocorrerá a revisão geral no próximo momento.
Por que a CP 911?
A partir de 2014 com a publicação da Lei 13.021 houve a atualização da Lei 5.991/73 – que visa muito o comércio de medicamentos e correlatos nas farmácias e drogarias –, houve ênfase nas atividades clínicas ofertados nas farmácias. Podemos evidenciar o Art. 2º “Farmácia é uma unidade de prestação de serviços destinados a prestar assistência farmacêutica, assistência à saúde e orientação sanitária individual e coletiva, na qual se processe a manipulação e/ou dispensação de medicamentos magistrais, oficinais, farmacopeicos ou industrializados, cosméticos, insumos farmacêuticos, produtos farmacêuticos e correlatos”.
A RDC 44/2009 limitava a assistência farmacêutica. Também sendo uma das motivações da atualização. O grande desafio é realizar a revisão de forma ampla, sob a óptica da vigilância sanitária e da coletividade. Portanto, o atendimento aos anseios individuais e/ou de grupos é um desafio.
Logo abaixo, apresento alguns pontos chaves das principais alterações propostas pela CP 911:
- Não haverá revogação da RDC 44/2009, portanto a mesma continuará com o mesmo número havendo apenas alterações no texto.
- O termo “drogaria” foi abolido e substituído por “farmácia” ora trazendo consigo também os termos “farmácias comunitárias privadas” e “farmácias comunitárias públicas”, se adequando à Lei 13.021/2014.
- O termo “uso racional de medicamentos” foi substituído por “uso seguro de medicamentos” em todo o texto da resolução.
- A RDC 50/2002 – que dispõe sobre o Regulamento Técnico para planejamento, programação, elaboração e avaliação de projetos físicos de estabelecimentos assistenciais de saúde – é mencionada como regulamento de referência para infraestrutura dos estabelecimentos que desempenham atividades de saúde (vide §1º Art. 15).
- Adoção da expressão “serviços de saúde”, o que pode ser observado logo no início na ementa proposta para a resolução e em todo o seu texto, em substituição ao termo “serviços farmacêuticos”. Destaco que o Art. 61 da nova proposta descreve que:
“Além da dispensação, as farmácias comunitárias podem oferecer serviços de saúde relacionados ao cuidado farmacêutico na atenção básica.”
Portanto, o trecho em negrito direciona os serviços de saúde ao cuidado farmacêutico apenas, não contemplando atividades alheias a este âmbito.
Segundo a Lei 13.021/2014 em seu Art. 13:
“Obriga-se o farmacêutico, no exercício de suas atividades, a:
I – notificar os profissionais de saúde e os órgãos sanitários competentes, bem como o laboratório industrial, dos efeitos colaterais, das reações adversas, das intoxicações, voluntárias ou não, e da farmacodependência observados e registrados na prática da farmacovigilância;
II – organizar e manter cadastro atualizado com dados técnico- científicos das drogas, fármacos e medicamentos disponíveis na farmácia;
III - proceder ao acompanhamento farmacoterapêutico de pacientes, internados ou não, em estabelecimentos hospitalares ou ambulatoriais, de natureza pública ou privada;
IV – estabelecer protocolos de vigilância farmacológica de medicamentos, produtos farmacêuticos e correlatos, visando a assegurar o seu uso racionalizado, a sua segurança e a sua eficácia terapêutica;
V – estabelecer o perfil farmacoterapêutico no acompanhamento sistemático do paciente, mediante elaboração, preenchimento e interpretação de fichas farmacoterapêuticas;
VI – prestar orientação farmacêutica, com vistas a esclarecer ao paciente a relação benefício e risco, a conservação e a utilização de fármacos e medicamentos inerentes à terapia, bem como as suas interações medicamentosas e a importância do seu correto manuseio.”.
Segundo o Caderno 1: Serviços Farmacêuticos na Atenção Básica (BRASIL, 2014), o cuidado farmacêutico na atenção básica, enquanto componente das ações de saúde, devem cumprir com as diretrizes propostas pela Política Nacional de Assistência Farmacêutica e representam um conjunto de procedimentos que podem ser organizados conforme demonstrado na figura abaixo:
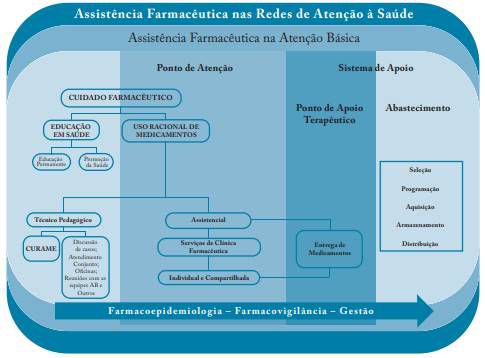
Fonte: Brasil, 2014.
O §1º do Art. 61 da nova proposta descreve que:
Os serviços de saúde oferecidos em farmácias comunitárias devem observar cumulativamente os requisitos e condições estabelecidas nas resoluções sanitárias destes serviços e nas políticas públicas relacionadas ao uso seguro de medicamentos.”
Com isso, o trecho em negrito deixa em aberto a possibilidade de haver serviços de saúde não contemplados na RDC 44, regulamentados por outros resoluções sanitárias e políticas públicas.
Isso também fica reforçado no inciso I do Art. 4º da CP 911 no qual revoga os §§2º e 5º do Art. 61 da RDC 44/2009. Tais parágrafos descrevem quais são os serviços de atenção farmacêutica exclusivamente, e a proibição da prestação de serviços não abrangidos na resolução, respectivamente.
Ademais, a CP 911 propõe no glossário a definição de serviço de saúde como “Atividade em que há prestação de assistência ao indivíduo ou à população humana que possa alterar o seu estado de saúde, objetivando a promoção, a prevenção, a recuperação ou a reabilitação da saúde, realizada obrigatoriamente por profissional de saúde ou sob sua supervisão”.
- Substituição do termo “serviço farmacêutico” e “atenção farmacêutica” por “cuidado farmacêutico”, de modo a estabelecer vínculo com a assistência farmacêutica definida pela Lei 13.021/2014.
- Revogação dos §§1º e 2º do Art. 69 da RDC 44/2009, os quais restringiam a aferição apenas da pressão arterial e da temperatura corporal como parâmetros fisiológicos, e a glicemia capilar como parâmetro bioquímico.
A pandemia do coronavírus, de certa forma, auxiliou este quesito, conforme já era previsto em normativas temporárias ainda vigentes: “Para fins do disposto no art. 1° da RDC nº 377, de 27 de abril de 2020, ficam suspensos o § 2° do art. 69 e o art. 70 da Resolução de Diretoria Colegiada - RDC n° 44, de 17 de agosto de 2009. A suspensão desses dispositivos se cessará automaticamente a partir do reconhecimento pelo Ministério da Saúde de que não mais se configura a Emergência em Saúde Pública de Importância Nacional declarada pela Portaria nº 188/GM/MS, de 4 de fevereiro de 2020”.
Com isso, a discussão trazida pelas entidades que representam os laboratório de análises clínicas é sobre qual o limite da assistência farmacêutica na aferição de parâmetros fisiológicos e bioquímicos por meio de dispositivos de apoio ao diagnóstico, tais como a utilização de POCT (Point-of-care Testing), adaptado ao Brasil como TLR (Teste Laboratorial Remoto) e TLP (Teste Laboratorial Portátil), que deveriam ser classificados com base num referencial de complexidade, com definição de critérios para que apenas tecnologias de baixa complexidade sejam oferecidas fora do ambiente laboratorial.
Vale lembrar que a RDC 302/2005 (laboratórios clínicos) apresenta uma definição de POCT conflitante e defasada em relação à definição da RDC 36/2015 (produtos de diagnóstico in vitro).
RDC 302/2005: “A execução dos Testes Laboratoriais Remotos – TLR (Point-of-care) e de testes rápidos, deve estar vinculada a um laboratório clínico, posto de coleta ou serviço de saúde pública ambulatorial ou hospitalar”.
RDC 36/2015: “point of care testing (PoCT): testagem conduzida próximo ao local de cuidado ao paciente, inclusive em consultórios e locais fora da área técnica de um laboratório, por profissionais de saúde ou por pessoal capacitado pelo Ministério da Saúde e ou Secretarias de Saúde Estaduais e Municipais”.
- O parágrafo único do Art. 71 da nova proposta descreve que:
“medição de parâmetros que demandem uma estrutura para o processamento, armazenamento ou transporte de amostras biológicas devem seguir o disposto no art. 18 da Lei 5.991/1973.”
O §2º do Art. 18 da Lei 5.991/73 descreve que:
“A farmácia poderá manter laboratório de análises clínicas, desde que em dependência distinta e separada, e sob a responsabilidade técnica do farmacêutico bioquímico.”
- O §2º do inciso I do Art. 81 da nova proposta não estabelece por quanto tempo deverá ser arquivado uma das vias da Declaração de Cuidado Farmacêutico na farmácia.
- Consultórios médicos e odontológicos especificados como ambientes proibidos em farmácia (vide Art. 90). Para resolver logo o imbróglio e a discussão sobre o famigerado “Consultório Farmacêutico”, ficaria mais claro se a nova proposta descrevesse neste artigo, ou até mesmo na Seção II - Do Ambiente Destinado aos Serviços de Saúde, que somente será permitida a utilização de consultório farmacêutico nas dependências da farmácia.
- Houve a inclusão do art. 1º- A, que traz uma lista de definições (glossário), as quais não eram descritas originalmente na RDC 44/09.
Há uma certa animosidade quanto a dois conceitos estabelecidos no glossário:
“Profissional legalmente habilitado: profissional com formação superior ou técnica com suas competências atribuídas por lei”.
“Responsável técnico: profissional legalmente habilitado, formalmente designado pelo responsável legal para manter as rotinas e os procedimentos de um serviço”.
Neste caso, não é especificado que o profissional legalmente habilitado deve estar inscrito em seu Conselho de classe. E o responsável técnico não cita o “farmacêutico” na sua descrição, já que a lei 13.021/14 é muito clara sobre o RT e foi a norma balizadora da revisão da RDC 44/09. - Inclusão do inciso VI no Art. 2º da nova proposta, prevendo o cadastro da farmácia no Cadastro Nacional de Estabelecimentos de Saúde – CNES, Acabando assim com a discussão discussão sobre a farmácia ser ou não ser estabelecimento de saúde.
CNES é o sistema de informação oficial de cadastramento de informações de todos os estabelecimentos de saúde no país, independentemente de sua natureza jurídica ou de integrarem o Sistema Único de Saúde (SUS). Trata-se do cadastro oficial do Ministério da Saúde (MS) no tocante à realidade da capacidade instalada e mão-de-obra assistencial de saúde no Brasil em estabelecimentos de saúde públicos ou privados, com convênio SUS ou não.
- Outro ponto importante foi a inclusão do Art. 61-A na nova proposta, cujo texto descreve que “As farmácias comunitárias devem garantir atendimento às intercorrências relacionadas aos serviços de saúde por elas prestados.”. Trouxe à tona a discussão sobre como as farmácias deverão se preparar para garantir este atendimento.
- Perfuração de lóbulo auricular (orelha) em seção específica, separando-a do serviço de saúde.
Todavia a CP 911 descreve no inciso XII do Art 3º “Ficam incluídos na Resolução de Diretoria Colegiada - RDC nº 44, de 2009:
o capítulo VI-A, com a seguinte redação:
Capítulo VI-A - Da Perfuração do Lóbulo Auricular para Colocação de Brincos.”.
A perfuração de lóbulo auricular para colocação de brincos já se encontra na Seção II de forma separada originalmente na RDC 44/2009.
Logo depois o inciso XIII até o XVI deste mesmo artigo coloca nos Art. 82-B, C, D, E os pontos relacionados à atividade supracitada, porém o Art. 82 originalmente faz parte da Seção III que trata sobre a Declaração de Serviços Farmacêuticos.
Houve a revogação da Seção II - Da Perfuração do Lóbulo Auricular para Colocação de Brincos, do Capítulo VI – DOS SERVIÇOS FARMACÊUTICOS da RDC 44/2009.
Além disso no inciso X do Art. 3º da CP 911, inclui a Seção III-A e o Art. 82-A para falar sobre das notificações para vigilância em saúde.
Em suma, ficou bem confuso.
- Criação da Seção III-A, específica sobre notificações de queixas técnicas, eventos adversos, incidentes e falhas na realização do serviço.
Este ponto vem reforçar a importância da Farmacovigilância e o infeliz cultura da subnotificação nas farmácias brasileiras. - Atualização das informações da Declaração de Serviços de Saúde prestados em farmácias (vide inciso VIII do Art. 3º da CP 911 – as alíneas i, j e k no inciso I do §2º do Art. 81 da RDC 44/2009).
“i) identificação do usuário ou do representante legal, quando for o caso, contendo: nome completo, data de nascimento (dia, mês e ano com quatro dígitos), sexo, naturalidade (indicando o município e o estado de nascimento), endereço completo (nome da via pública, número, complemento, bairro/distrito, município, estado e CEP);
“j) descrição da queixa do usuário; e
k) descrição dos serviços de saúde prestados.”. - Revogação do Art. 62 da RDC 44/2009, que determina que o “estabelecimento deve manter disponível, para informar ao usuário, lista atualizada com a identificação dos estabelecimentos públicos de saúde mais próximos, contendo a indicação de endereço e telefone.”.
- Todos os estabelecimentos terão 90 dias a partir da publicação da atualização da norma para se adequarem.
Ismael Rosa – Farmacêutico, Diretor Acadêmico do ICTQ. Mestrando em Ciências Farmacêuticas. Especialista em Vigilância Sanitária na Indústria Farmacêutica. Especialista em Prescrição Farmacêutica e Farmácia Clínica. Conselheiro suplente do CRF-GO. Membro da Comissão Assessora de Indústria Farmacêutica do CRF-GO.









